Селективный ингибитор семейства янус-киназ
Торговые наименования и формы выпуска
- Тофацитиниб: таблетки, покрытые пленочной оболочкой (5 мг, 10 мг)
- Тофара: таблетки, покрытые пленочной оболочкой (5 мг, 10 мг)
- Яквинус:
- таблетки, покрытые пленочной оболочкой (5 мг, 10 мг)
- таблетки с модифицированным высвобождением, покрытые пленочной оболочкой, 11 мг
- раствор для приема внутрь, 1 мг/мл
- Тофацитиниб Фармасинтез: таблетки, покрытые пленочной оболочкой (5 мг, 10 мг)
Механизм действия
Тофацитиниб представляет собой мощный, селективный ингибитор семейства янус-киназ, обладающий высокой селективностью в отношении прочих киназ генома человека. По результатам исследования киназ тофацитиниб ингибирует янус-киназы 1, 2, 3 и в меньшей степени – тирозин-киназу-2. В тех клетках, где янус-киназы передают сигнал парами, тофацитиниб предпочтительно ингибирует передачу сигнала гетеродимерных рецепторов, связанных с янус-киназой-3 и/или янус-киназой-1, обладая функциональной селективностью в отношении рецепторов, которые передают сигналы через пары янус- киназы-2. Ингибирование янус-киназы-1 и янус-киназы-3 под действием тофацитиниба блокирует передачу сигнала посредством общих рецепторов, содержащих гамма-цепи, в отношении нескольких цитокинов, включая ИЛ-2, -4, -7, -9, -15 и -21. Эти цитокины выполняют интегрирующую роль в процессах активации лимфоцитов, их пролиферации, функционирования и торможения передачи сигнала, что приводит к модулированию разнообразных аспектов иммунного ответа. Кроме того, ингибирование янус-киназы-1 приводит к ослаблению передачи сигнала под действием дополнительных провоспалительных цитокинов, таких как ИЛ-6 и ИФН-γ. При более высокой экспозиции препарата ингибирование передачи сигнала янус-киназы-2 приводит к ингибированию передачи сигнала эритропоэтина.
Как ингибитор янус-киназы-1/тирозин-киназы-2-зависимой передачи сигналов ИФНα, тофацитиниб будет модулировать выработку и действие ИФНα. Тофацитиниб также напрямую ингибирует передачу сигналов ИЛ-6, важного медиатора лихорадки и реагентов острой фазы, и некоторых цитокинов (а именно, ИЛ-15, ИЛ-21, ИЛ-23), что, в свою очередь, снижает количество цитокинов, выделяемых Т-хелперными клетками 17 типа (т.е. ФНОα, ИЛ-17а, ИЛ-17f, ИЛ-22), которые участвуют в патогенезе острого респираторного дистресс-синдрома (ОРДС). Кроме того, тофацитиниб напрямую подавляет передачу сигналов ИФНγ, ИЛ-2 и ИЛ 12, участвующих в дифференцировке Т-хелперных клеток 1 типа, что, в свою очередь, снижает количество цитокинов, высвобождаемых клетками Т- хелперными клетками 1 типа (т.е. ФНОα, ИЛ-2, ИФНγ). Таким образом, ожидается, что действие тофацитиниба на нескольких контрольных точках уменьшит многие провоспалительные пути, ведущие к прогрессирующему повреждению легких, проявлению новой коронавирусной инфекции, вызванной COVID-19.
Показания к применению
Таблетки
- Ревматоидный артрит
- Тофацитиниб показан для лечения взрослых пациентов с умеренным или тяжелым активным ревматоидным артритом с неадекватным ответом на один или несколько базисных противовоспалительных препаратов (БПВП).
- Псориатический артрит
- Тофацитиниб показан для лечения взрослых пациентов с активным псориатическим артритом с неадекватным ответом на один или несколько БПВП.
- Анкилозирующий спондилоартрит
- Тофацитиниб показан для лечения взрослых пациентов с активным анкилозирующим спондилоартритом (АС) с неадекватным ответом на традиционную терапию.
- Бляшечный псориаз
- Тофацитиниб показан для лечения взрослых с хроническим бляшечным псориазом умеренной или тяжелой степени выраженности, когда показана системная терапия или фототерапия.
- Язвенный колит
- Тофацитиниб показан для индукционной и поддерживающей терапии взрослых пациентов с умеренным или тяжелым активным язвенным колитом (ЯК) с недостаточным ответом, потерей ответа или непереносимостью кортикостероидов, азатиоприна (АЗТ), 6-меркаптопурина (6-МП) или ингибиторов фактора некроза опухолей (ФНО).
- Полиартикулярный ювенильный идиопатический артрит
- Тофацитиниб показан для лечения активного полиартикулярного ювенильного идиопатического артрита (пЮИА) у пациентов в возрасте 2 лет и старше.
- Новая коронавирусная инфекция, вызванная COVID-19
- Новая коронавирусная инфекция, вызванная COVID-19 у госпитализированных взрослых пациентов с легким/среднетяжелым течением и факторами риска тяжелого течения при наличии патологических изменений в легких, соответствующих КТ1-2, но не получающих инвазивную или неинвазивную вентиляцию или экстракорпоральную мембранную оксигенацию (ЭКМО).
Раствор для приема внутрь
Яквинус показан к применению у детей в возрасте от 2-х лет и старше и у подростков до 18 лет по следующим показаниям:
- лечение активного полиартикулярного ювенильного идиопатического артрита (полиартрит с положительным [RF+] или отрицательным [RF–] результатом анализа на ревматоидный фактор и распространенный олигоартрит) при неадекватном ответе на предыдущую терапию базисными противовоспалительными препаратами (БПВП);
- ювенильного псориатического артрита (ПсА) при неадекватном ответе на предыдущую терапию БПВП.
Тофацитиниб может назначаться в комбинации с метотрексатом (МТ) или в качестве монотерапии при непереносимости МТ или нецелесообразности дальнейшей терапии МТ.
Противопоказания
Таблетки
- гиперчувствительность к тофацитинибу или к любому из вспомогательных веществ, перечисленных в разделе 6.1;
- тяжелое нарушение функции печени;
- инфицирование вирусами гепатита В и/или С (наличие серологических маркеров HBV и HCV инфекции);
- клиренс креатинина менее 40 мл/мин;
- одновременное применение живых вакцин;
- следует избегать одновременного применения препарата Тофацитиниб Фармасинтез с биологическими препаратами, такими как, ингибиторы фактора некроза опухоли (ФНО), антагонисты интерлейкинов (ИЛ-IR, ИЛ-6R), моноклональные анти-CD20 антитела, антагонисты ИЛ-17, антагонисты ИЛ-12/ИЛ-23, антиинтегрины, селективные ко-стимулирующие модуляторы, а также мощные иммунодепрессанты, такие как азатиоприн, циклоспорин и такролимус, поскольку такая комбинация увеличивает вероятность выраженной иммуносупрессии и риск развития инфекции;
- тяжелые инфекции, активные инфекции, включая локальные, тяжелые инфекционные заболевания;
- беременность (безопасность и эффективность не исследовались);
- период грудного вскармливания.
Тофацитиниб 10 мг два раза в сутки противопоказан пациентам, у которых есть одно или несколько из следующих состояний:
- Использование комбинированных гормональных контрацептивов или заместительной гормональной терапии.
- Сердечная недостаточность.
- Венозная тромбоэмболия в анамнезе, а именно тромбоэмболия глубоких вен или легочная эмболия.
- Наследственное нарушение свертываемости крови.
- Злокачественное новообразование.
- Пациенты, подвергающиеся значительным хирургическим вмешательствам.
Препарат Тофацитиниб Фармасинтез следует применять с осторожностью:
- при повышенном риске перфорации органов желудочно-кишечного тракта (ЖКТ) (например, у пациентов с дивертикулитом в анамнезе).
- у лиц пожилого возраста и пациентов с сахарным диабетом в связи с высоким риском развития инфекционных заболеваний.
Раствор для приема внутрь
Применение препарата Яквинус противопоказано при:
- Гиперчувствительности к действующему веществу или к любому из вспомогательных веществ, перечисленных в разделе 6.1.
- Активной форме туберкулеза (ТБ), серьезных инфекциях, таких как сепсис, или оппортунистические инфекции (см. раздел 4.4).
- Тяжелом нарушении функции печени (см. раздел 4.2).
- Беременности и лактации (см. раздел 4.6).
Применение при беременности и в период лактации
Таблетки
Беременность
Адекватные, хорошо контролируемые исследования применения тофацитиниба у беременных женщин не проводились. Тофацитиниб не следует принимать во время беременности (см. раздел 4.3).
Лактация
Способность тофацитиниба проникать в грудное молоко человека не изучена. В доклинических исследованиях тофацитиниб выделялся в молоко крыс. Поскольку риск для новорожденных и грудных детей не может быть исключен, применение тофацитиниба противопоказано в период грудного вскармливания (см. раздел 4.3).
Женщины с детородным потенциалом/Контрацепция у женщин
Женщинам с детородным потенциалом следует рекомендовать использование эффективных средств контрацепции во время терапии тофацитинибом и в течение по меньшей мере 4 недель после приема последней дозы препарата.
Раствор для приема внутрь
Беременность
Адекватные, хорошо контролируемые исследования применения тофацитиниба у беременных женщин не проводились. Было выявлено тератогенное действие тофацитиниба и воздействие на роды и перинатальное и постнатальное развитие у крыс и кроликов (см. раздел 5.3).
В качестве меры предосторожности применение тофацитиниба во время беременности противопоказано (см. раздел 4.3).
Женщины, способные к деторождению/ Контрацепция у женщин
Женщинам с репродуктивным потенциалом следует рекомендовать использование эффективных средств контрацепции во время терапии тофацитинибом и в течение по меньшей мере 4 недель после приема последней дозы препарата.
Лактация
Способность тофацитиниба проникать в грудное молоко у человека не изучена. Нельзя исключать наличия риска для ребенка, находящегося на грудном вскармливании. Тофацитиниб выделялся с молоком кормящих крыс (см. раздел 5.3). В качестве меры предосторожности применение тофацитиниба в период кормления грудью противопоказано (см. раздел 4.3).
Фертильность
Формальные исследования потенциального влияния препарата на репродуктивную функцию человека не проводились. Тофацитиниб нарушал репродуктивную функцию у самок крыс, но не нарушал репродуктивную функцию у самцов (см. раздел 5.3).
Способ применения и дозы
Таблетки
- Внутрь вне зависимости от приема пищи.
Режим дозирования
Взрослые
Анкилозирующий спондилоартрит
- Рекомендованная доза составляет 5 мг два раза в день.
Ревматоидный артрит
- Тофацитиниб можно применять в качестве монотерапии или в комбинации с метотрексатом или другими небиологическими БПВП.
- Рекомендованная доза составляет 5 мг два раза в день.
- У некоторых пациентов может потребоваться увеличение дозы до 10 мг два раза в день, в зависимости от клинического ответа на терапию.
- Две таблетки препарата Тофацитиниб Фармасинтез 5 мг биоэквивалентны одной таблетке препарата Тофацитиниб Фармасинтез 10 мг и могут использоваться в качестве альтернативы одной таблетке препарата Тофацитиниб Фармасинтез 10 мг.
Псориатический артрит
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг два раза в сутки в комбинации со стандартными синтетическими БМАРП (ссБМАРП).
Бляшечный псориаз
- Рекомендованная доза препарата Тофацитиниб Фармасинтез для лечения бляшечного псориаза умеренной или тяжелой степени составляет 10 мг два раза в сутки (также см. подраздел «Особые группы пациентов»).
- Две таблетки препарата Тофацитиниб Фармасинтез 5 мг биоэквивалентны одной таблетке препарата Тофацитиниб Фармасинтез 10 мг и могут использоваться в качестве альтернативы одной таблетке препарата Тофацитиниб Фармасинтез 10 мг.
Язвенный колит
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез для лечения взрослых пациентов с умеренным или тяжелым активным язвенным колитом составляет 10 мг перорально два раза в сутки для индукционной терапии в течение не менее 8 недель, затем 5 мг или 10 мг два раза в сутки для поддерживающей терапии в зависимости от терапевтического ответа.
- Две таблетки препарата Тофацитиниб Фармасинтез 5 мг биоэквивалентны одной таблетке препарата Тофацитиниб Фармасинтез 10 мг и могут использоваться в качестве альтернативы одной таблетке препарата Тофацитиниб Фармасинтез 10 мг.
- Индукционную терапию прекращают у пациентов, не достигших терапевтического эффекта к 16 неделе.
- Для рефрактерных пациентов, таких как пациенты, которые не ответили на предыдущую терапию ингибитором ФНО, следует рассмотреть вопрос о продолжении лечения с применением поддерживающей дозы 10 мг два раза в сутки.
- Пациенты, для которых не сохранился терапевтический эффект препарата Тофацитиниб Фармасинтез в дозе 5 мг два раза в сутки, он может быть достигнут с помощью приема препарата Тофацитиниб Фармасинтез в дозе 10 мг два раза в сутки.
- В целом, следует применять самую низкую эффективную дозу для поддержания терапевтического эффекта.
Новая коронавирусная инфекция, вызванная COVID-19
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез для взрослых пациентов составляет 10 мг два раза в сутки в течение 14 дней.
- Тофацитиниб должен применяться только у госпитализированных пациентов и под наблюдением врачей-специалистов, имеющих опыт лечения данного заболевания.
- Если выписка из стационара происходит до завершения 14-дневного периода лечения, прием тофацитиниба следует прекратить.
- Две таблетки препарата Тофацитиниб Фармасинтез 5 мг биоэквивалентны одной таблетке препарата Тофацитиниб Фармасинтез 10 мг и могут использоваться в качестве альтернативы одной таблетке препарата Тофацитиниб Фармасинтез 10 мг.
Коррекция дозы в связи с лабораторными отклонениями
- Может потребоваться коррекция дозы или прекращение терапии в случае развития дозозависимых отклонений лабораторных показателей, включая лимфопению, нейтропению и анемию (см. табл. 1, 2 и 3).
- Не рекомендуется начинать терапию у пациентов с абсолютным числом нейтрофилов (АЧН) менее 1000/мм3 или с уровнем гемоглобина менее 9 г/дл.
- Для показания «Новая коронавирусная инфекция, вызванная COVID-19» не рекомендуется начинать терапию препаратом у пациентов с количеством лимфоцитов менее 500 клеток/мм3.
Таблица 1. Коррекция дозы при лимфопении
| Сниженное число лимфоцитов (см. раздел 4.4) | |
| Результат анализа (клеток/мм3) | Рекомендации |
| Число лимфоцитов ≥ 500 | Без изменений |
| Число лимфоцитов < 500 (подтверждено повторным анализом) | Прекращение лечения |
Таблица 2. Коррекция дозы при нейтропении
| Низкое значение АЧН (см. раздел 4.4) | |
| Лабораторное значение (клеток/мм3) | Рекомендации |
| АЧН >1000 | Без изменений |
| АЧН 500-1000 | При стойком снижении в этом диапазоне, следует снизить дозу или отменить прием до достижения АЧН более 1000 клеток/мм3. Для пациентов, получающих тофацитиниб в дозе 5 мг два раза в сутки, приостановить прием препарата. При АЧН более 1000 |
| клеток/мм3 возобновить прием тофацитиниба в дозе 5 мг два раза в сутки. Для пациентов, получающих тофацитиниб в дозе 10 мг два раза в сутки, уменьшить дозу препарата до 5 мг два раза в сутки. При АЧН более 1000 клеток/мм3 увеличить прием тофацитиниба в дозе 10 мг два раза в сутки, основываясь на клиническом ответе на лечение. | |
| АЧН <500 (подтверждено при повторной оценке) | Прекращение лечения |
Таблица 3. Коррекция дозы при анемии
| Низкое значение гемоглобина (см. раздел 4.4) | |
| Лабораторное значение (г/дл) | Рекомендации |
| ≥ 9,0 г/дл и снижение на 2 г/дл или менее | Без изменений |
| < 8,0 г/дл или снижение более чем на 2 г/дл (подтверждено при повторной оценке) | Следует прекратить применение препарата Тофацитиниб Фармасинтез до нормализации гемоглобина. |
Особые категории пациентов
Пациенты пожилого возраста (≥ 65 лет)
- Коррекция дозы у пациентов в возрасте 65 лет и старше не требуется.
Пациенты с нарушением функции почек
- Если дозировка препарата Тофацитиниб Фармасинтез составляет 5 мг два раза в сутки, рекомендованная доза для пациентов с тяжелыми нарушениями функции почек составляет 5 мг один раз в сутки (см. разделы 4.4 и 5). Конкретные рекомендации для каждого показания представлены ниже.
- Если дозировка препарата Тофацитиниб Фармасинтез составляет 10 мг два раза в сутки, рекомендованная доза для пациентов с тяжелыми нарушениями функции почек составляет 5 мг два раза в сутки (см. разделы 4.4 и 5). Конкретные рекомендации для каждого показания представлены ниже.
Ревматоидный артрит
- Пациентам с нарушением функции почек легкой или средней степени тяжести не требуется коррекции дозы.
- Доза препарата Тофацитиниб Фармасинтез не должна превышать 5 мг два раза в день у пациентов с тяжелым нарушением функции почек (включая, но не ограничиваясь, пациентов, находящихся на гемодиализе).
Псориатический артрит
- У пациентов с нарушениями функции почек легкой или умеренной степени коррекция дозы препарата не требуется.
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов с тяжелыми нарушениями почечной функции (включая, но не ограничиваясь, пациентов, находящихся на гемодиализе) (см. разделы 4.4 и 5).
Анкилозирующий спондилоартрит
- У пациентов с нарушениями функции почек легкой или средней степени коррекция дозы препарата не требуется.
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов с тяжелой почечной недостаточностью (включая, но не ограничиваясь, пациентов, находящихся на гемодиализе) (см. разделы 4.4 и 5).
Бляшечный псориаз
- У пациентов с нарушениями функции почек легкой или умеренной степени коррекция дозы препарата не требуется.
- У пациентов с нарушениями функции почек тяжелой степени доза препарата Тофацитиниб Фармасинтез не должна превышать 5 мг два раза в сутки (включая, но не ограничиваясь, пациентов, находящихся на гемодиализе) (см. разделы 4.4 и 5).
Язвенный колит
- У пациентов с нарушениями функции почек легкой или умеренной степени коррекция дозы препарата не требуется.
- Для пациентов с тяжелыми нарушениями почечной функции (включая, но не ограничиваясь, пациентов, находящихся на гемодиализе) рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг два раза в сутки, если при нормальной почечной функции пациенту было бы назначено 10 мг два раза в сутки, рекомендуемая доза составляет 5 мг один раз в сутки если бы при нормальной почечной функции пациенту было бы назначено 5 мг два раза в сутки.
Полиартикулярный ювенильный идиопатический артрит
- У пациентов с нарушениями функции почек легкой или умеренной степени коррекции дозы не требуется. Для пациентов с тяжелыми нарушениями почечной функции (включая, но не ограничиваясь, пациентов, находящихся на гемодиализе) рекомендуемая доза препарата
- Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки, если бы при нормальной почечной функции пациенту было бы назначено 5 мг два раза в сутки (см. разделы 4.4 и 5).
Новая коронавирусная инфекция, вызванная COVID-19
- У пациентов с нарушениями функции почек умеренной или тяжелой степени коррекция дозы необходима (см. таблицу 4 ниже). У пациентов с нарушениями функции почек легкой степени коррекция дозы препарата не требуется.
Пациенты с нарушением функции печени
- У пациентов с нарушениями функции печени легкой степени тяжести коррекция дозы препарата не требуется.
- Если дозировка препарата Тофацитиниб Фармасинтез составляет 5 мг два раза в сутки, рекомендованная доза для пациентов с нарушениями печеночной функции умеренной степени составляет 5 мг один раз в сутки.
- Если дозировка препарата Тофацитиниб Фармасинтез составляет 10 мг два раза в сутки, рекомендованная доза для пациентов с нарушениями печеночной функции умеренной степени составляет 5 мг два раза в сутки.
- Конкретные рекомендации для каждого показания представлены ниже.
Ревматоидный артрит
- У пациентов с нарушениями функции печени легкой степени тяжести коррекция дозы препарата не требуется.
- Не следует применять Тофацитиниб Фармасинтез у пациентов с тяжелым нарушением функции печени.
- Доза препарата Тофацитиниб Фармасинтез не должна превышать 5 мг два раза в день у пациентов с нарушением функции печени средней степени тяжести.
Псориатический артрит
- У пациентов с нарушениями функции печени легкой степени тяжести коррекция дозы препарата не требуется.
- Препарат Тофацитиниб Фармасинтез не рекомендуется принимать пациентам с тяжелыми нарушениями функции печени.
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов с нарушениями печеночной функции умеренной степени (см. разделы 4.4 и 5).
Анкилозирующий спондилоартрит
- У пациентов с нарушениями функции печени легкой степени тяжести коррекция дозы препарата не требуется.
- Препарат Тофацитиниб Фармасинтез не рекомендуется принимать пациентам с тяжелыми нарушениями функции печени.
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов с нарушениями печеночной функции средней степени (см. разделы 4.4 и 5).
Бляшечный псориаз
- У пациентов с нарушениями функции печени легкой степени коррекция дозы препарата не требуется.
- Препарат Тофацитиниб Фармасинтез не рекомендуется принимать пациентам с тяжелыми нарушениями функции печени.
- У пациентов с нарушениями функции печени умеренной степени доза препарата Тофацитиниб Фармасинтез не должна превышать 5 мг два раза в сутки (см. разделы 4.4 и 5).
Язвенный колит
- У пациентов с нарушениями функции печени легкой степени коррекция дозы препарата не требуется.
- Препарат Тофацитиниб Фармасинтез не рекомендуется принимать пациентам с тяжелыми нарушениями функции печени.
- Для пациентов с нарушениями печеночной функции умеренной степени рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг два раза в сутки, если рекомендуемая доза при нормальной печеночной функции составляет 10 мг два раза в сутки, рекомендуемая доза составляет 5 мг один раз в сутки при рекомендуемой дозе 5 мг два раза в сутки при нормальной печеночной функции.
Полиартикулярный ювенильный идиопатический артрит
- У пациентов с нарушениями функции печени легкой степени коррекция дозы препарата не требуется.
- Препарат Тофацитиниб Фармасинтез не рекомендуется принимать пациентам с тяжелыми нарушениями функции печени.
- Для пациентов с нарушениями печеночной функции средней степени рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки, если рекомендуемая доза при нормальной печеночной функции составляет 5 мг два раза в сутки (см. разделы 4.4 и 5).
Новая коронавирусная инфекция, вызванная COVID-19
- Препарат Тофацитиниб Фармасинтез не рекомендуется принимать пациентам с тяжелыми нарушениями функции печени.
- Рекомендации по дозировке препарата для пациентов с нарушениями функции печени легкой или средней степени представлены в таблице 4 ниже.
Таблица 4. Критерии коррекции дозы/Временного прекращения лечения/Прекращения леченияа
| Лабораторный показатель/ Состояние/ Взаимодействие | Значение | Рекомендации |
| Лабораторные отклонения | ||
| Абсолютное число лимфоцитов | ≥ 250 клеток/мм3 | Без изменений |
| < 250 клеток/мм3 | Прекращение лечения | |
| Абсолютное число нейтрофилов | ≥ 500 клеток/мм3 | Без изменений |
| < 500 клеток/мм3 | Прекращение лечения | |
| Гемоглобин | ≥ 8,0 г/дл < 8,0 г/дл | Без изменений Прекращение лечения |
| Уровень трансаминаз | АЛТ или АСТ < 5 × ВГН | Без изменений |
| АЛТ или АСТ ≥ 5 × ВГН | Временно прекратить лечение, провести обследование и рассмотреть возможность отмены тофацитиниба | |
| Белые кровяные клетки | ≥ 1000 клеток/мм3 | Без изменений |
| < 1000 клеток/мм3 | Прекращение лечения | |
| Особые категории пациентов | ||
| Нарушение функции печени | ||
| Нарушение функции печени легкой степени | Без изменений | |
| Нарушение функции печени средней степени | 5 мг два раза в сутки | |
| Нарушение функции почек | ||
| Нарушение функции почек легкой степени (рСКФ) ≥ 60 мл/мин/1,73 м2 и < 90 мл/мин/1,73 м2) | Без изменений | |
| Нарушение функции почек тяжелой степени (рСКФ) < 30 мл/мин/1,73 м2) или средней степени (рСКФ < 60 мл/мин/1,73 м2) | 5 мг два раза в сутки | |
| Лекарственные взаимодействия | ||
| Одновременное применение с сильными ингибиторами CYP3A4, или комбинацией умеренного ингибитора CYP3A4 и сильного ингибитора CYР2С19 | 5 мг два раза в сутки | |
Сокращения: АЛТ – аланинаминотрансфераза, АСТ – аспартатаминотрансфераза, рСКФ – расчетная скорость клубочковой фильтрации, ВГН – верхняя граница нормы.
а Если лабораторное отклонение связано, вероятно, с основным заболеванием, следует рассмотреть риски и пользу продолжения приема тофацитиниба в той же или сниженной дозе.
Одновременное применение с ингибиторами цитохрома Р450 (CYP3A4) и изоферментом CYP2C19
- Для показаний с максимальной рекомендуемой дозой препарата Тофацитиниб Фармасинтез 5 мг два раза в сутки для пациентов, получающих сильные ингибиторы CYP3A4 (например, кетоконазол) или один или более сопутствующих препаратов, что приводит в обоих случаях к умеренному ингибированию CYP3A4 и сильному ингибированию CYP2C19 (например, флуконазол), рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки.
- Конкретные рекомендации для каждого показания представлены ниже.
Ревматоидный артрит
- У пациентов, получающих мощные ингибиторы изофермента CYP3A4 (например, кетоконазол), доза препарата Тофацитиниб Фармасинтез не должна превышать 5 мг один раз в день.
- У пациентов, получающих один или несколько сопутствующих препаратов, способных умеренно ингибировать изофермент CYP3A4 и активно ингибировать изофермент СYР2С19 (например, флуконазол), доза препарата Тофацитиниб Фармасинтез не должна превышать 5 мг один раз в сутки.
Псориатический артрит
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов, получающих сильные ингибиторы СYР3А4 (например, кетоконазол).
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов, получающих один или более сопутствующих препаратов, что приводит в обоих случаях к умеренному ингибированию СYР3А4 и сильному ингибированию CYP2C19 (например, флуконазол).
Анкилозирующий спондилоартрит
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов, получающих сильные ингибиторы СYР3А4 (например, кетоконазол).
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в сутки для пациентов, получающих один или более сопутствующих препаратов, что приводит в обоих случаях к умеренному ингибированию СYР3А4 и сильному ингибированию CYP2C19 (например, флуконазол).
Бляшечный псориаз
- Дозировка препарата Тофацитиниб Фармасинтез не должна превышать 5 мг два раза в сутки для пациентов, получающих сильные ингибиторы СYР3А4 (например, кетоконазол).
- Дозировка препарата Тофацитиниб Фармасинтез не должна превышать 5 мг два раза в сутки для пациентов, получающих один или более сопутствующих препаратов, что приводит в обоих случаях к умеренному ингибированию СYР3А4 и сильному ингибированию CYP2C19 (например, флуконазол).
Язвенный колит
- Для пациентов, получающих сильные ингибиторы СYР3А4 (например, кетоконазол) или один или более сопутствующих препаратов, что приводит в обоих случаях к умеренному ингибированию СYР3А4 и сильному ингибированию СYР2С19 (например, флуконазол), дозу препарата Тофацитиниб Фармасинтез следует уменьшить до 5 мг два раза в сутки, если пациент принимает 10 мг два раза в сутки, дозу препарата Тофацитиниб Фармасинтез следует уменьшить до 5 мг один раз в сутки, если пациент принимает 5 мг два раза в сутки.
Полиартикулярный ювенильный идиопатический артрит
- У пациентов, получающих сильные ингибиторы СYР3А4 (например, кетоконазол) или один или более сопутствующих препаратов, которые приводят как к умеренному ингибированию СYР3А4, так и к сильному ингибированию CYP2C19 (например, флуконазол), рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг один раз в день, если доза при нормальной функции почек составляет 5 мг два раза в день (см. разделы 4.4 и 5).
Одновременное применение с индукторами цитохрома Р450 (СYР3А4)
- Одновременное применение препарата Тофацитиниб Фармасинтез и мощных индукторов изофермента СYР3А4 (например, рифампицина) может приводить к снижению или утрате клинической эффективности (см. раздел 4.5).
- Одновременное применение препарата Тофацитиниб Фармасинтез и мощных индукторов изофермента СYР3А4 не рекомендуется.
Бляшечный псориаз у пациентов японской и корейской национальностей
- У пациентов данной категории повышен риск развития опоясывающего герпеса.
- Следует рассмотреть возможность применения препарата в дозе 5 мг два раза в сутки.
Дети
Полиартикулярный ювенильный идиопатический артрит
- Препарат Тофацитиниб Фармасинтез может применяться в качестве монотерапии или в комбинации с метотрексатом.
- Рекомендуемая доза препарата Тофацитиниб Фармасинтез составляет 5 мг два раза в сутки (см. таблицу 5 ниже).
Таблица 5. Рекомендуемая дозировка препарата Тофацитиниб Фармасинтез для пациентов с пЮИА в возрасте 2 лет и старше
| Масса тела (кг) | Режим дозирования |
| ≥40 | 5 мг два раза в сутки |
- Эффективность и безопасность тофацитиниба в дозировке 5 мг два раза в день оценивалась у пациентов с пЮИА в возрасте от 2 лет до 18 лет.
- Безопасность и эффективность тофацитиниба у детей в возрасте менее 2 лет с пЮИА не установлены. Данные отсутствуют.
Другое
- Безопасность и эффективность тофацитиниба у детей в возрасте менее 18 лет по другим показаниям не установлены. Данные отсутствуют.
Раствор для приема внутрь
- Для приема внутрь.
- Тофацитиниб раствор для приема внутрь следует принимать с помощью прилагаемого адаптера для флакона и шприца для перорального введения.
- Тофацитиниб принимают внутрь независимо от приема пищи.
- Лечение должно назначаться и контролироваться врачами-специалистами, имеющими опыт диагностики и лечения состояний, при которых показано применение тофацитиниба.
Режим дозирования
- Тофацитиниб можно применять в качестве монотерапии или в комбинации с МТ.
- Рекомендуемая доза препарата для лечения пациентов в возрасте 2 лет и старше зависит от массы тела.
Таблица 1. Доза тофацитиниба для лечения пациентов с полиартикулярным ювенильным идиопатическим артритом и ювенильным ПсА в возрасте 2 лет и старше
| Масса тела (кг) | Режим дозирования |
| От 10 до < 20 | 3,2 мг (3,2 мл раствора для приема внутрь) два раза в день |
| От 20 до < 40 | 4 мг (4 мл раствора для приема внутрь) два раза в день |
| ≥ 40 | 5 мг (5 мл раствора для приема внутрь или 5 мг в виде таблетки, покрытой пленочной оболочкой) два раза в день |
- Пациенты с массой тела ≥ 40 кг, получающие тофацитиниб в форме раствора для приема внутрь в дозе 5 мл два раза в день, могут быть переведены на лечение тофацитинибом в форме таблеток, покрытых пленочной оболочкой, в дозе 5 мг два раза в день.
- Пациенты с массой тела < 40 кг не могут быть переведены с лечения тофацитинибом в форме раствора для приема внутрь.
Коррекция дозы
- При применении в комбинации с МТ коррекция дозы препарата не требуется.
Временное или полное прекращение терапии
- Согласно имеющимся данным клиническое улучшение наблюдается в течение 18 недель после начала лечения тофацитинибом.
- При отсутствии улучшения у пациента в течение указанного срока следует провести тщательную повторную оценку целесообразности продолжения терапии.
- При развитии у пациента серьезной инфекции лечение тофацитинибом следует приостановить до установления контроля над инфекцией.
- Может потребоваться временное прекращение терапии в случае развития дозозависимых отклонений лабораторных показателей, включая лимфопению, нейтропению и анемию. Рекомендации по временному или полному прекращению терапии, приведенные в таблицах 2, 3 и 4 ниже, зависят от степени тяжести отклонений от нормы результатов лабораторных показателей (см. раздел 4.4).
- Не рекомендуется начинать терапию препаратом у детей с абсолютным числом лимфоцитов (АЧЛ) менее 750 клеток/мм3.
Таблица 2. Низкое абсолютное число лимфоцитов
| Низкое абсолютное число лимфоцитов (АЧЛ) (см. раздел 4.4) | |
| Лабораторный показатель (клеток/мм3) | Рекомендация |
| АЧЛ 750 и более | Доза остается на прежнем уровне. |
| АЧЛ 500–750 | При стойком снижении в этом диапазоне (2 определенных подряд значения в пределах этого диапазона при стандартном лабораторном исследовании) следует снизить дозу или отменить прием до достижения АЧЛ более 750. Для пациентов, получающих тофацитиниб в дозе 5 мг два раза в день, следует приостановить прием препарата. При достижении АЧЛ более 750, терапию следует возобновить в соответствии с клинической целесообразностью. |
| АЧЛ менее 500 | Если величина лабораторного показателя подтверждается при повторном анализе в течение 7 дней, применение препарата должно быть прекращено. |
- Не рекомендуется начинать терапию препаратом у детей с абсолютным числом нейтрофилов (АЧН) менее 1200 клеток/мм3.
Таблица 3. Низкое абсолютное число нейтрофилов
| Низкое абсолютное число нейтрофилов (АЧН) (см. раздел 4.4) | |
| Лабораторный показатель (клеток/мм3) | Рекомендация |
| АЧН более 1000 | Доза остается без изменений. |
| АЧН 500–1000 | При стойком снижении в этом диапазоне (2 определенных подряд значения в пределах этого диапазона при стандартном лабораторном исследовании) следует снизить дозу или отменить прием до достижения АЧН более 1000. Для пациентов, получающих тофацитиниб в дозе 5 мг два раза в день, следует приостановить прием препарата. При достижении АЧН более 1000, терапию следует возобновить в соответствии с клинической целесообразностью. |
| АЧН менее 500 | Если величина лабораторного показателя подтверждается при повторном анализе в течение 7 дней, применение препарата должно быть прекращено. |
- Не рекомендуется начинать терапию препаратом у детей с уровнем гемоглобина менее 10 г/дл.
Таблица 4. Низкое значение гемоглобина
| Низкое значение гемоглобина (см. раздел 4.4) | |
| Лабораторный показатель (г/дл) | Рекомендация |
| Снижение не более чем на 2 г/дл или уровень не менее 9,0 г/дл | Доза остается без изменений. |
| Снижение более чем на 2 г/дл или уровень менее 8,0 г/дл (подтверждено при повторном анализе) | Следует прекратить применение препарата до нормализации уровня гемоглобина. |
Взаимодействия
- У пациентов, получающих тофацитиниб в дозе 5 мг (таблетка, покрытая пленочной оболочкой) два раза в сутки или в эквивалентной дозе, рассчитанной по массе тела, два раза в сутки, и при этом получающих мощные ингибиторы цитохрома P450 (CYP) 3A4 (например, кетоконазол), или один или более сопутствующих препаратов, которые приводят как к умеренному ингибированию изофермента CYP3A4, так и к мощному ингибированию изофермента CYP2C19 (например флуконазол), общая суточная доза тофацитиниба должна быть снижена до 5 мг (таблетка, покрытая пленочной оболочкой) один раз в день или до эквивалентной дозы, рассчитанной по массе тела, один раз в день (см. раздел 4.5).
Таблица 5. Коррекция дозы раствора при одновременном применении с ингибиторами цитохрома P450 (CYP3A4) и изоферментом CYP2C19
| Степень мощности ингибитора изоферментов | Коррекция дозы раствора |
| Пациенты, получающие: мощные ингибиторы изофермента CYP3A4 (например, кетоконазол) или умеренные ингибиторы изофермента CYP3A4 с мощными ингибиторами изофермента CYP2C19 (например, флуконазол) | Если пациент принимает дозу 3,2 мг два раза в день, следует уменьшить ее до 3,2 мг один раз в день. Если пациент принимает дозу 4 мг два раза в день, следует уменьшить ее до 4 мг один раз в день. Если пациент принимает дозу 5 мг два раза в сутки, следует уменьшить ее до 5 мг один раз в сутки. |
Особые группы пациентов
Лица пожилого возраста
- Безопасность и эффективность тофацитиниба, раствор для приема внутрь, у пожилых пациентов не установлены.
Пациенты с печеночной недостаточностью
Таблица 6. Коррекция дозы при нарушении функции печени
| Степень нарушения функции печени | Классификация | Коррекция дозы раствора для приема внутрь при нарушении функции печени |
| Легкая степень | Класс A по шкале Чайлд — Пью | Коррекция дозы не требуется. |
| Умеренная степень | Класс B по шкале Чайлд — Пью | Если пациент принимает дозу 3,2 мг два раза в день, следует уменьшить ее до 3,2 мг один раз в день. Если пациент принимает дозу 4 мг два раза в день, следует уменьшить ее до 4 мг один раз в день. Если рекомендуемая доза при нормальной функции печени составляет 5 мг или эквивалент этой дозы, рассчитанный по массе тела, два раза в день, следует уменьшить дозу до 5 мг или эквивалента этой дозы, рассчитанного по массе тела, один раз в день (см. раздел 5.2). |
| Тяжелая степень | Класс C по шкале Чайлд — Пью | Тофацитиниб не рекомендуется принимать пациентам с тяжелым нарушением функции печени (см. раздел 4.3). |
Пациенты с почечной недостаточностью
Таблица 7. Коррекция дозы при нарушении функции почек
| Степень нарушения функции почек | Клиренс креатинина | Коррекция дозы раствора для приема внутрь при нарушении функции почек |
| Легкая степень | 50–80 мл/мин | Коррекция дозы не требуется. |
| Умеренная степень | 30–49 мл/мин | Если пациент принимает дозу 3,2 мг два раза в день, следует уменьшить ее до 3,2 мг один раз в день. Если пациент принимает дозу 4 мг два раза в день, следует уменьшить ее до 4 мг один раз в день. |
| Тяжелая степень (включая пациентов, находящихся на гемодиализе) | < 30 мл/мин | Если пациент принимает дозу 3,2 мг два раза в день, следует уменьшить ее до 3,2 мг один раз в день. Если пациент принимает дозу 4 мг два раза в день, следует уменьшить ее до 4 мг один раз в день. Если рекомендуемая доза при нормальной функции почек составляет 5 мг или эквивалент этой дозы, рассчитанный по массе тела, два раза в день, следует уменьшить дозу до 5 мг или эквивалента этой дозы, рассчитанного по массе тела, один раз в день. Пациенты с тяжелым нарушением функции почек должны продолжать получать препарат в сниженной дозе даже после гемодиализа (см. раздел 5.2). |
Дети (младше 2 лет)
- Безопасность и эффективность тофацитиниба у детей младше 2 лет не установлены. Данные отсутствуют.
Взаимодействие с другими лекарственными средствами
Таблетки
Взаимодействия, влияющие на применение тофацитиниба
Поскольку тофацитиниб метаболизируется под действием изофермента СYР3А4, весьма вероятно взаимодействие с препаратами, которые ингибируют или индуцируют данный изофермент. При одновременном применении с мощными ингибиторами изофермента СYР3А4 (например, кетоконазолом), а также при одновременном применении с одним или несколькими умеренными ингибиторами изофермента СYР3А4 и мощными ингибиторами изофермента CYP2C19 (например, флуконазолом) экспозиция тофацитиниба увеличивается (см. раздел 4.2). Одновременное применение кетоконазола (мощного ингибитора изофермента СYР3А4) и однократной дозы тофацитиниба повышает AUC и Сmax тофацитиниба на 103 % и 16 %, соответственно. Одновременное применение флуконазола (умеренного ингибитора изофермента СYР3А4, а также мощного ингибитора изофермента CYP2C19) увеличивает AUC и Сmax тофацитиниба на 79 % и 27 %, соответственно.
При одновременном применении тофацитиниба с сильным ингибитором изофермента СYР3А4 или комбинацией умеренного ингибитора изофермента СYР3А4 и сильного ингибитора изофермента СYР2С19 необходима коррекция дозы тофацитиниба (см. раздел 4.2).
При одновременном применении с мощными индукторами изофермента СYР3А4 (например, рифампицином) экспозиция тофацитиниба уменьшается. Одновременное применение рифампицина (мощного индуктора изофермента СYР3А4) снижает AUC и Сmax тофацитиниба на 84 % и 74 %, соответственно (см. раздел 4.2).
Вероятность влияния ингибиторов изофермента CYP2C19 или Р-гликопротеина на фармакокинетику тофацитиниба мала.
Применение тофацитиниба не рекомендуется у пациентов, принимающих мощный индуктор изофермента СYР3А4 (например, рифампицин, зверобой продырявленный) или у пациентов, которые прекратили прием мощного индуктора изофермента СYР3А4 менее чем за 28 дней или 5 периодов полувыведения до приема первой дозы тофацитиниба.
Одновременное применение такролимуса (слабого ингибитора изофермента СYР3А4) увеличивает AUC тофацитиниба на 21 % и снижает Сmax тофацитиниба на 9 %. Одновременное применение циклоспорина (умеренного ингибитора изофермента СYР3А4) увеличивает AUC тофацитиниба на 73 % и снижает Сmax тофацитиниба на 17 %.
Одновременное многократное применение тофацитиниба и мощных иммунодепрессантов у пациентов с ревматоидным артритом, псориазом, псориатическим артритом, анкилозирующим спондилоартритом, язвенным колитом или полиартикулярным ювенильным идиопатическим артритом не изучалось.
Одновременное применение с метотрексатом (15–25 мг метотрексата один раз в неделю) не оказывает влияния на фармакокинетику тофацитиниба.
Взаимодействия, при которых тофацитиниб влияет на фармакокинетику других препаратов Исследования in vitro показали, что тофацитиниб в концентрациях, даже более чем в 80 раз превышающих равновесную Сmax общего тофацитиниба, возникающую при применении 5 мг и 10 мг два раза в день тофацитиниба у пациентов с ревматоидным артритом, псориатическим артритом, псориазом, язвенным колитом и полиартикулярным ювенильным идиопатическим артритом, существенно не ингибирует и не индуцирует активность основных препаратов, метаболизируемых цитохромами (СYР1А2, СYР2В6, СYР2С8, СYР2С9, СYР2С19, CYP2D6 и СYР3А4). Данные результаты были подтверждены исследованиями in vitro лекарственного взаимодействия, которые показали отсутствие изменений фармакокинетики мидазолама, высокоселективного субстрата изофермента СYР3А4, при одновременном применении с тофацитинибом.
Данные in vitro показывают, что тофацитиниб не ингибирует активность основного человеческого фермента, метаболизирующего лекарственные средства, уридин 5- дифосфат-глюкуронозилтрансферазы (УГТ) [УГТ1А1, УГТ1А4, УГТ1А6, УГТ1А9 и УГТ2В7], в концентрациях, в 250 раз превышающих равновесную Сmax общего тофацитиниба, возникающую при применении 5 мг и 10 мг два раза в день тофацитиниба у пациентов с ревматоидным артритом, псориатическим артритом, псориазом, язвенным колитом и полиартикулярным ювенильным идиопатическим артритом.
Данные in vitro показали, что способность тофацитиниба в терапевтических концентрациях ингибировать такие переносчики как Р-гликопротеин, органические анионные транспортные полипептиды, органические анионные или катионные переносчики очень низка.
Одновременное применение с тофацитинибом не оказывало влияния на фармакокинетику пероральных контрацептивов, левоноргестрела и этинилэстрадиола у здоровых женщин. Одновременное применение тофацитиниба с метотрексатом в дозе 15–25 мг один раз в неделю снижало показатели AUC и Сmax метотрексата на 10 % и 13 %, соответственно. Данные изменения фармакокинетики метотрексата не требовали коррекции дозы, либо подбора индивидуальных доз метотрексата.
У пациентов с ревматоидным артритом, псориазом, язвенным колитом и полиартикулярным ювенильным идиопатическим артритом клиренс тофацитиниба с течением времени не изменялся. Это свидетельствует о том, что тофацитиниб не влияет на активность изоферментов СYР у этих пациентов. Таким образом, маловероятно, что одновременное применение субстратов изоферментов СYР с тофацитинибом приведет к клинически значимому увеличению их метаболизма у пациентов с ревматоидным артритом, псориазом, язвенным колитом и полиартикулярным ювенильным идиопатическим артритом. Сопутствующий прием тофацитиниба не оказывал влияния на фармакокинетику метформина, свидетельствуя, что тофацитиниб не воздействует на переносчик органических катионов (ОСТ2) у здоровых добровольцев.
Раствор для приема внутрь
Возможное влияние других лекарственных препаратов на фармакокинетику (ФК) тофацитиниба
Поскольку тофацитиниб метаболизируется под действием изофермента CYP3A4, весьма вероятно взаимодействие с лекарственными препаратами, которые ингибируют или индуцируют данный изофермент. При одновременном применении с мощными ингибиторами изофермента CYP3A4 (например, кетоконазолом), а также при одновременном применении с одним или несколькими умеренными ингибиторами изофермента CYP3A4 и мощными ингибиторами изофермента CYP2C19 (например, флуконазолом) экспозиция тофацитиниба увеличивается (см. раздел 4.2).
Экспозиция тофацитиниба уменьшается при его одновременном применении с мощными индукторами изоферментами CYP (например, рифампицином). Вероятность существенного влияния ингибиторов изофермента CYP2C19 или Р-гликопротеина на фармакокинетику тофацитиниба мала.
Одновременное применение кетоконазола (мощного ингибитора изофермента CYP3A4), флуконазола (умеренного ингибитора изофермента CYP3A4 и мощного ингибитора изофермента CYP2C19), такролимуса (слабого ингибитора изофермента CYP3A4) и циклоспорина (умеренного ингибитора изофермента CYP3A4) повышает AUC тофацитиниба, тогда как его одновременное применение с рифампицином (мощным индуктором CYP) снижает AUC тофацитиниба. Одновременное применение тофацитиниба с мощными индукторами CYP (например, рифампицином) может приводить к потере или снижению клинического ответа на терапию (см. рисунок 1). Одновременное применение тофацитиниба и мощных индукторов изофермента CYP3A4 не рекомендуется. При одновременном применении с кетоконазолом и флуконазолом наблюдалось повышение Cmax тофацитиниба, тогда как при одновременном применении с такролимусом, циклоспорином и рифампицином наблюдалось снижение его Cmax. Одновременное применение с МТ в дозе 15–25 мг один раз в неделю не оказывает влияния на фармакокинетику тофацитиниба у пациентов с РА (см. рисунок 1).
Рисунок 1. Влияние других лекарственных препаратов на фармакокинетику (ФК) тофацитиниба
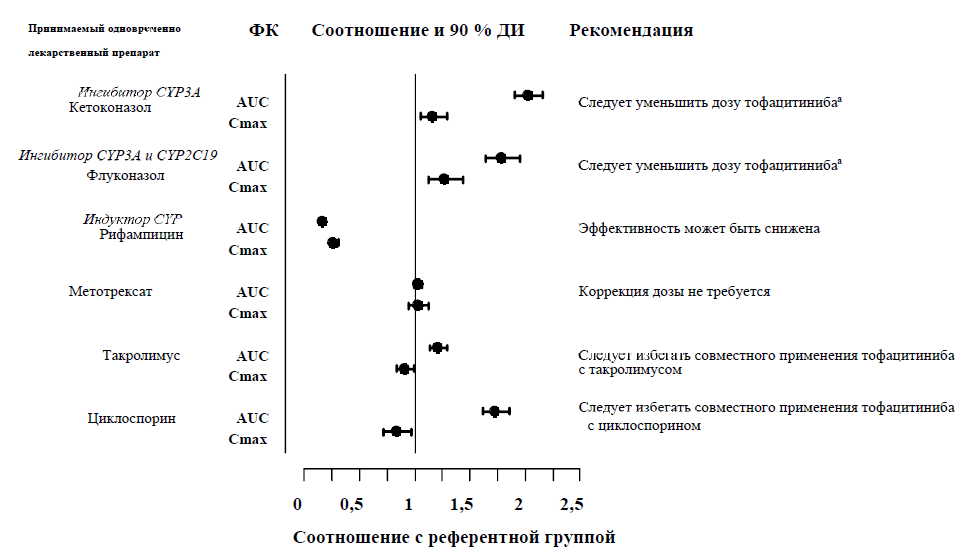
Примечание. Референтная группа принимала тофацитиниб в качестве монотерапии.
а У пациентов, получающих препарат в дозе 5 мг или эквивалентной дозе, рассчитанной по массе тела, два раза в день, дозу тофацитиниба следует уменьшить до 5 мг в форме таблеток, покрытых пленочной оболочкой, или раствора для приема внутрь в эквивалентной дозе, рассчитанной по массе тела, один раз в день (см. раздел 4.2).
Возможное влияние тофацитиниба на ФК других лекарственных препаратов
Одновременное применение с тофацитинибом не оказывало влияния на ФК пероральных контрацептивов, левоноргестрела и этинилэстрадиола у здоровых женщин-добровольцев.
Одновременное применение тофацитиниба с МТ в дозе 15–25 мг один раз в неделю снижало показатели AUC и Cmax МТ на 10 % и 13 % соответственно у пациентов с РА. Данные изменения фармакокинетики метотрексата не требовали коррекции дозы, либо подбора индивидуальных доз метотрексата.
Дети
Исследования взаимодействия проведены только у взрослых.
Особые указания
Таблетки
Тофацитиниб не изучался и его применения следует избегать у пациентов с ослабленным иммунитетом, с подтвержденными иммунодефицитными состояниями или у пациентов, принимающих сильнодействующие иммунодепрессанты (например, азатиоприн, циклоспорин), другие ингибиторы янус-киназ или биологические препараты, направленные на цитокины, В-клетки или Т-клетки, из-за возможности усиления иммуносупрессии и повышения риска инфекции.
Пациенты, получающие активное лечение по поводу любого злокачественного новообразования или лимфопролиферативного заболевания, не должны получать тофацитиниб.
Комбинированное применение с другими противоревматическими средствами Применение тофацитиниба не изучалось и его применения следует избегать у пациентов с ревматоидным артритом в комбинации с биологическими базисными противоревматическими препаратами (БПРП), такими как ингибиторы фактора некроза опухоли (ФНО), антагонисты интерлейкина (ИЛ)-1R, антагонисты ИЛ-6R, моноклональные антитела к CD-20, селективные модуляторы ко-стимуляции и высокоактивные иммунодепрессанты, например, азатиоприн, циклоспорин и такролимус, поскольку существует риск усиления иммуносупрессии с последующим увеличением риска развития инфекции.
При применении тофацитиниба в комбинации с МТТ наблюдалась более высокая частота нежелательных явлений, чем при применении тофацитиниба в виде монотерапии.
Применение тофацитиниба не изучалось и его применения следует избегать у пациентов пЮИА в комбинации с биологическими базисными противоревматическими препаратами (БПРП), такими как антагонисты ИЛ-6R, селективные модуляторы ко-стимуляции и высокоактивными иммунодепрессантами, например, азатиоприн и циклоспорин, поскольку существует риск усиления иммуносупрессии с последующим увеличением риска развития инфекции.
Применение тофацитиниба не изучалось и его применения следует избегать у пациентов с анкилозирующим спондилоартритом в комбинации с биологическими базисными противоревматическими препаратами (БПРП) или высокоактивными иммунодепрессантами, например, азатиоприн и циклоспорин.
Общие инфекции
Наиболее частыми инфекциями, отмечаемыми на фоне применения тофацитиниба у пациентов с ревматоидным артритом, были инфекции верхних дыхательных путей и назофарингит (4,1 % и 3,4 %, соответственно).
Наиболее частыми инфекциями, отмечаемыми в течение первых 12-16 недель терапии тофацитинибом пациентов с псориазом, были назофарингит и инфекции верхних дыхательных путей (назофарингит в 7 % и 8 % случаев при применении 5 мг и 10 мг тофацитиниба два раза в сутки, соответственно и инфекции верхних дыхательных путей в 4 % и 5 % случаев при применении 5 мг и 10 мг тофацитиниба два раза в сутки, соответственно).
Серьезные инфекции
У пациентов, получающих иммуномодуляторы, включая биологические препараты и тофацитиниб, отмечены серьезные, а иногда и смертельные инфекции, вызванные бактериальными, микобактериальными, грибковыми, вирусными или иными оппортунистическими возбудителями. Самые частые серьезные инфекции, отмеченные при применении тофацитиниба, включают пневмонию, инфекцию мочевыводящих путей, воспаление подкожной клетчатки, опоясывающий герпес, бронхит, септический шок, дивертикулит, гастроэнтерит, аппендицит и сепсис. Из числа оппортунистических инфекций при применении тофацитиниба отмечены случаи развития туберкулеза и других микобактериальных инфекций, криптококкоза, гистоплазмоза, кандидоза пищевода, опоясывающего лишая с поражением различных дерматомов, цитомегаловирусной инфекции, ВК-вирусной инфекции и листериоза. У некоторых пациентов с ревматоидным артритом отмечали диссеминированные заболевания чаще всего при одновременном применении иммуномодуляторов – метотрексата или глюкокортикостероидов, которые сами по себе и в дополнение к основному заболеванию ревматоидному артриту могут предрасполагать к развитию инфекций. Также возможно развитие и иных серьезных инфекций, которые не были зарегистрированы в клинических исследованиях (например, кокцидиомикоза).
В одном крупном рандомизированном пострегистрационном исследовании безопасности (PASS) у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний у пациентов, получавших тофацитиниб, по сравнению с ингибитором ФНО наблюдалось дозозависимое увеличение числа серьезных инфекций. Некоторые из этих серьезных инфекций привели к смертельному исходу. В исследовании также сообщалось об оппортунистических инфекциях.
За исключением новой коронавирусной инфекции, вызванной COVID-19, тофацитиниб не следует назначать пациентам с подозреваемыми или подтвержденными активными системными бактериальными, грибковыми или вирусными инфекциями, включая, помимо прочего, активную инфекцию опоясывающего герпеса; подтвержденный активный туберкулез или историю неадекватно леченного туберкулеза; подтвержденные HBV, HCV или ВИЧ инфекции. Перед применением тофацитиниба следует оценить соотношение риск/польза от терапии у пациентов с активными серьезными инфекциями, кроме новой коронавирусной инфекции, вызванной COVID-19, с хронической или рецидивирующей инфекцией, после контакта с больным туберкулезом, наличием тяжелой или оппортунистической инфекции в анамнезе, у пациентов, которые жили или недавно посетили эндемичные районы по туберкулезу или микозам, а также у пациентов с предрасположенностью к развитию инфекции. Пациенты подлежат внимательному наблюдению на предмет развития признаков и симптомов инфекции во время и после терапии тофацитинибом. Тофацитиниб следует временно отменить, если у пациента развилась серьезная инфекция, оппортунистическая инфекция или сепсис, до тех пор, пока не будет установлен контроль над состоянием пациента. При развитии новой инфекции на фоне применения тофацитиниба пациент подлежит быстрому и полному диагностическому обследованию по аналогии с пациентом, страдающим иммунодефицитом. Показано назначение соответствующей антибактериальной терапии, а также тщательное динамическое наблюдение.
Поскольку пожилые пациенты и пациенты с сахарным диабетом обычно характеризуются более высокой частотой развития инфекций, в подобных случаях также следует соблюдать осторожность. Также рекомендуется соблюдать осторожность при применении препарата у пациентов с хроническими заболеваниями легких, так как они могут быть более подвержены инфекциям. В клинических исследованиях и во время пострегистрационного применения препарата сообщалось о случаях развития интерстициального заболевания легких (в некоторых случаях с летальным исходом) у пациентов, получающих терапию тофацитинибом, ингибитором янус-киназ. Тем не менее, роль ингибирования янус-киназы неизвестна.
Риск инфекции может повышаться при увеличении степени тяжести лимфопении. В этом случае при оценке индивидуального риска развития инфекции следует принимать во внимание количество лимфоцитов. Условия отмены препарата и критерии контроля лимфопении описаны в разделе 4.2.
Туберкулез
Перед применением тофацитиниба следует оценить соотношение риск/польза от терапии у пациентов с туберкулезом в анамнезе, у пациентов, которые жили или недавно посетили эндемичные районы по туберкулезу.
Перед применением тофацитиниба следует провести обследование на предмет признаков латентной или активной туберкулезной инфекции в соответствии с локальными рекомендациями.
Пациенты с латентным туберкулезом перед началом терапии тофацитинибом подлежат стандартной антимикобактериальной терапии.
Перед началом терапии тофацитинибом у пациентов с латентным или активным туберкулезом в анамнезе, при отсутствии подтверждения адекватного курса противотуберкулезной терапии, а также у пациентов с отрицательным результатом исследования на латентный туберкулез, но наличием факторов риска туберкулезной инфекции, следует провести соответствующую противотуберкулезную терапию. При принятии решения относительно необходимости проведения противотуберкулезной терапии у каждого конкретного пациента рекомендуется проконсультироваться с фтизиатром.
Пациенты подлежат тщательному наблюдению на предмет развития признаков туберкулеза, включая пациентов с отрицательным результатом теста на латентный туберкулез до начала терапии.
Реактивация вирусных инфекций
Реактивация вирусных инфекций описана при применении терапии БПВП. Случаи реактивации вируса герпеса (например, опоясывающего герпеса) также описаны в клинических исследованиях тофацитиниба. В одном крупном рандомизированном пострегистрационном исследовании безопасности (PASS) у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно- сосудистых заболеваний у пациентов, получавших тофацитиниб, наблюдалось увеличение случаев опоясывающего герпеса по сравнению с ингибитором ФНО. В постмаркетинговых исследованиях сообщалось о случаях реактивации вируса гепатита В у пациентов, получавших терапию тофацитинибом. Влияние тофацитиниба на реактивацию хронического вирусного гепатита неизвестно. Пациентов с положительным результатом тестирования на гепатиты В и С исключили из клинических исследований. Перед началом терапии тофацитинибом следует провести скрининг на предмет наличия вирусного гепатита.
В клинических исследованиях тофацитиниба у представителей японской и корейской национальностей отмечаются более частые случаи развития опоясывающего герпеса, чем у представителей других национальностей.
Частота появления опоясывающего герпеса может увеличиться у пациентов с длительным анамнезом ревматоидного артрита, которые ранее получали два и более биологических БПВП; у пациентов с АЧН менее 1000 клеток/мм3.
Венозная тромбоэмболия
Венозная тромбоэмболия (ВТЭ) наблюдалась у пациентов, принимавших тофацитиниб в клинических исследованиях и пострегистрационных отчетах. В одном крупном рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет или старше, с хотя бы одним дополнительным сердечно-сосудистым фактором риска, пациенты получали лечение тофацитинибом в дозе 5 мг два раза в сутки, тофацитинибом в дозе 10 мг два раза в сутки или ингибитором ФНО. В данном исследовании наблюдалось дозозависимое повышение частоты развития легочной эмболии (ЛЭ) у пациентов, которые получали терапию тофацитинибом в сравнении с терапией ингибиторами ФНО (см. раздел 4.8). Многие случаи ЛЭ были серьезными и некоторые случаи имели летальный исход.
Случаи ЛЭ в этом исследовании были зарегистрированы чаще у пациентов, принимающих тофацитиниб, по сравнению с другими исследованиями тофацитиниба (см. раздел 4.8).
Случаи тромбоза глубоких вен (ТГВ) наблюдались во всех трех группах пациентов данного исследования (см. раздел 4.8).
Необходимо проводить оценку пациентов относительно факторов риска венозных тромбоэмболических явлений до начала лечения и периодически во время лечения. Необходимо применять тофацитиниб с осторожностью у пожилых пациентов и у пациентов, имеющих другие факторы риска (см. раздел 4.2). Необходимо безотлагательно проводить оценку пациентов с признаками и симптомами ВТЭ и отменить тофацитиниб у пациентов с подозреваемым ВТЭ, вне зависимости от применяемой дозы или показания.Тофацитиниб не изучался, и его применения следует избегать у пациентов с тромбозом в анамнезе или подтвержденным тромбозом в настоящий момент времени, а также у пациентов с нарушением свертываемости крови в личном и семейном анамнезе первой степени родства.
Тофацитиниб следует применять только у взрослых госпитализированных пациентов с новой коронавирусной инфекцией, вызванной COVID-19, которые получают антикоагулянтную профилактику ВТЭ. Не следует применять эстрогенсодержащие контрацептивы в течение 48 часов до начала лечения или во время лечения. При появлении клинических признаков тромбоза глубоких вен/эмболии легочной артерии прием тофацитиниба следует прекратить, пациентов следует незамедлительно обследовать и назначить соответствующее лечение.
Основные нежелательные сердечно-сосудистые события (включая инфаркт миокарда)
В одном крупном рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно- сосудистых заболеваний пациенты получали тофацитиниб 5 мг два раза в день, тофацитиниб 10 мг два раза в день или ингибитор ФНО. Основные неблагоприятные сердечно-сосудистые события (МАСЕ), включая инфаркт миокарда, наблюдались во всех трех группах лечения в этом исследовании. У пациентов, получавших тофацитиниб, по сравнению с ингибитором ФНО наблюдалось увеличение числа нефатальных инфарктов миокарда. МАСЕ, включая, инфаркт миокарда, чаще встречались у пожилых пациентов и пациентов, которые курят в настоящее время или в прошлом. Следует проявлять осторожность при лечении пожилых пациентов, пациентов, которые курят в настоящее время или в прошлом, а также пациентов с другими факторами риска сердечно-сосудистых заболеваний.
Злокачественные и лимфопролиферативные заболевания (за исключением рака кожи, не относящийся к меланоме (РКНМ))
Перед началом терапии пациентов с существующим злокачественным новообразованием или данными о злокачественном новообразовании в анамнезе, кроме излеченного немеланомного рака кожи (НМРК), или при рассмотрении возможности продолжения терапии тофацитинибом у пациентов со злокачественным новообразованием следует учитывать риски и преимущества лечения тофацитинибом. Существует возможность, что тофацитиниб влияет на защиту организма от злокачественных новообразований.
Анкилозирующий спондилоартрит
В комбинированной популяции безопасности, состоящей из 1 плацебо-контролируемого клинического исследования фазы 2 и 1 плацебо-контролируемого клинического исследования фазы 3 среди пациентов с активным анкилозирующим спондилоартритом у 420 пациентов, получавших тофацитиниб до 48 недель (233 пациенто-лет наблюдения), не были выявлены злокачественные новообразования, за исключением рака кожи, не относящегося к меланоме (РКНМ).
У пациентов, получавших лечение тофацитинибом, были зарегистрированы случаи лимфомы и у пациентов, получавших тофацитиниб в большом рандомизированном исследовании PASS, у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний. Несмотря на то, что у пациентов с ревматоидным артритом, особенно с высокоактивной формой заболевания, и у пациентов с псориазом может наблюдаться более высокий риск (в несколько раз выше) развития лимфомы по сравнению с общей популяцией, роль тофацитиниба, если таковая имеется, в развитии лимфомы не установлена.
Рак легких наблюдался у пациентов, получавших тофацитиниб. Рак легких также наблюдался у пациентов, получавших тофацитиниб, в большом рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний; увеличение случаев рака легких наблюдалось у пациентов, получавших тофацитиниб 10 мг два раза в день по сравнению с ингибитором ФНО. Из 30 случаев рака легких, зарегистрированных в исследовании у пациентов, принимавших тофацитиниб, все, кроме 2, были у пациентов, которые курили в настоящее время или в прошлом. Пациенты с ревматоидным артритом могут подвергаться более высокому риску развития рака легких, чем общая популяция.
В клинических исследованиях и пострегистрационном периоде были зарегистрированы случаи развития других злокачественных новообразований, включая (но не ограничиваясь), рак груди, меланома, рак предстательной железы и рак поджелудочной железы.
Влияние терапии тофацитинибом на развитие и течение злокачественных новообразований неизвестно.
Следует соблюдать осторожность при лечении пациентов пожилого возраста, пациентов, которые курят или курили в прошлом, а также пациентов с другими факторами риска злокачественных новообразований.
В большом рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний наблюдалось увеличение злокачественных новообразований (за исключением РКНМ) у пациентов, получавших тофацитиниб, по сравнению с ингибитором ФНО). Злокачественные новообразования (за исключением РКНМ) чаще встречались у пожилых пациентов и у пациентов, которые курили в настоящее время или в прошлом.
Рак кожи, не относящийся к меланоме (РКНМ)
Сообщалось о случаях развития РКНМ у пациентов, получающих терапию тофацитинибом. РКНМ также были зарегистрированы в большом рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний. В этом исследовании у пациентов, получавших тофацитиниб, по сравнению с ингибитором ФНО, наблюдалось увеличение общего количества РКНМ, включая плоскоклеточный рак кожи. Поскольку частота РКНМ выше у пожилых людей и у пациентов с анамнезом РКНМ, следует соблюдать осторожность при лечении таких пациентов. Рекомендуется проводить периодическое обследование кожи у пациентов с повышенным риском развития рака кожи.
Тофацитиниб в дозировке 10 мг два раза в день противопоказан пациентам с высоким риском легочной эмболии (см. раздел 4.3). Дополнительными факторами риска, которые следует учитывать при определении риска развития ЛЭ у пациента, являются пожилой возраст, ожирение, курение и иммобилизация.
Случаи перфорации органов ЖКТ
В клинических исследованиях в том числе в большом рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше, по крайней мере, с одним дополнительным фактором риска сердечно-сосудистых заболеваний описаны случаи перфорации органов ЖКТ. Роль ингибирования янус-киназы при этих явлениях неизвестна. Такие случаи в основном были описаны как перфорация дивертикула, перитонит, абсцесс в брюшной полости и аппендицит. Все пациенты с ревматоидным артритом, у которых развилась перфорация органов ЖКТ, получали сопутствующую терапию нестероидными противовоспалительными препаратами (НПВП) и/или глюкокортикоидами. Относительный вклад сопутствующей терапии и применения тофацитиниба при развитии перфорации органов ЖКТ неизвестен. Частота развития таких осложнений у пациентов с псориазом, согласно данным клинических исследований, составляет 0,09 случаев/100 пациенто-лет.
Тофацитиниб следует с осторожностью применять у пациентов с повышенным риском перфорации органов ЖКТ (например, у пациентов с дивертикулитом в анамнезе). Пациенты с новыми симптомами со стороны органов ЖКТ подлежат немедленному обследованию для раннего выявления перфорации органов ЖКТ. В клинических исследованиях анкилозирующего спондилоартрита не было выявлено случаев перфорации органов ЖКТ среди 420 пациентов, получавших тофацитиниб в течение до 48 недель (233 пациенто-лет наблюдения).
Переломы
Переломы наблюдались у пациентов, получавших тофацитиниб в клинических исследованиях и в пострегистрационный период.
В контролируемых клинических исследованиях фазы 3 у пациентов с РА в течение периода от 0 до 3 месяцев частота переломов у пациентов, получавших тофацитиниб 5 мг два раза в день, тофацитиниб 10 мг два раза в день и плацебо составляла 2,11, 2,56 и 4,43 пациентов с событиями на 100 PYs, соответственно.
В большом рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше по крайней мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний переломы наблюдались в группах лечения тофацитинибом и ингибиторами ФНО.
Следует проявлять осторожность у пациентов с известными факторами риска переломов, таких как пожилые пациенты, пациенты женского пола и пациенты, принимающие кортикостероиды.
Риск сердечно-сосудистых заболеваний
Пациенты с ревматоидным артритом подвержены повышенному риску возникновения нарушений со стороны сердечно-сосудистой системы, и у таких пациентов следует контролировать факторы риска (например, артериальную гипертензию и гиперлипидемию) в рамках обычного стандартного лечения.
Ферменты печени
При лечении тофацитинибом у некоторых пациентов наблюдалось увеличение частоты повышения уровней печеночных ферментов. Следует с вниманием подходить к вопросу о начале лечения тофацитинибом у пациентов с повышенными уровнями аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (АСТ), особенно при начале применения препарата в комбинации с потенциально гепатотоксичными лекарственными препаратами, такими как метотрексат. После начала лечения для выявления потенциальных случаев лекарственного поражения печени рекомендуется осуществлять на постоянной основе контроль биохимических показателей функции печени и быстро устанавливать возможные причины повышения уровней печеночных ферментов. Если подозревается лекарственное поражение печени, лечение тофацитинибом следует приостановить до исключения этого диагноза.
Гиперчувствительность
У пациентов, принимающих тофацитиниб, наблюдались такие реакции гиперчувствительности как ангионевротический отек и крапивница. Некоторые случаи оценивались как серьезные. Большинство реакций возникало у пациентов с множественной аллергией в анамнезе. В случае возникновения серьезной реакции гиперчувствительности необходимо немедленно прекратить применение тофацитиниба до выявления потенциальной причины или причин. Пациенты с подтвержденной аллергией на тофацитиниб не должны принимать препарат.
Лабораторные показатели
Лимфоциты: случаи снижения числа лимфоцитов до уровня менее 500 клеток/мм3 были связаны с увеличением частоты серьезных инфекций, которые потребовали терапии. Не рекомендуется начинать терапию тофацитинибом у пациентов с низким числом лимфоцитов (т.е. менее 500 клеток/мм3). Если у пациента подтверждено снижение абсолютного числа лимфоцитов до уровня менее 500 клеток/мм3, лечение тофацитинибом не рекомендуется. Уровень лимфоцитов необходимо контролировать на исходном уровне и затем каждые 3 месяца (см. раздел 4.2).
Нейтрофилы: лечение тофацитинибом сопровождалось увеличением частоты развития нейтропении (< 2000 клеток/мм3) по сравнению с плацебо. Начинать лечение тофацитинибом пациентов с низкой концентрацией нейтрофилов (АЧН менее 1000 клеток/мм3) не рекомендуется. У пациентов, получающих тофацитиниб в дозировке 10 мг два раза в день, со стойким снижением АЧН до 500–1000 клеток/мм3 следует снизить дозу тофацитиниба до 5 мг два раза в день до достижения концентрации АЧН более 1000 клеток/мм3. У пациентов, получающих тофацитиниб в дозировке 5 мг два раза в день, со стойким снижением АЧН до 500–1000 клеток/мм3 следует прекратить лечение до достижения концентрации АЧН более 1000 клеток/мм3. У пациентов с подтвержденным абсолютным числом нейтрофилов менее 500 клеток/мм3 лечение не рекомендуется. Уровень нейтрофилов следует контролировать на исходном уровне и после 4–8 недель терапии, а затем каждые 3 месяца (см. разделы 4.2, 4.8).
Гемоглобин: не рекомендуется начинать терапию тофацитинибом у пациентов с низким уровнем гемоглобина (менее 9 г/дл). Лечение тофацитинибом следует прекратить у пациентов с уровнем гемоглобина менее 8 г/дл, либо при снижении уровня гемоглобина на 2 г/дл и более на фоне лечения. Гемоглобин следует контролировать на начальном этапе терапии, после 4–8 недель терапии, а затем каждые 3 месяца (см. раздел 4.2).
Липиды: лечение тофацитинибом сопровождается повышением уровня липидов крови – общего холестерина, холестерина ЛПНП, а также холестерина липопротеидов высокой плотности (ЛПВП). Максимальный эффект обычно отмечался в течение 6 недель. Повышение общего холестерина, холестерина ЛПНП и холестерина ЛПВП также было зарегистрировано в большом рандомизированном исследовании PASS у пациентов с РА в возрасте 50 лет и старше, по крайней мере, с одним дополнительным фактором риска сердечно-сосудистых заболеваний. Оценку липидных параметров следует выполнять по прошествии около 4–8 недель после начала терапии. Применение статинов у пациентов с повышенной концентрацией общего холестерина и холестерина ЛПНП на фоне терапии тофацитинибом позволяет достичь исходных показателей.
Вакцинации
Информация по вторичной трансмиссии инфекции при введении живых вакцин пациентам, получающим тофацитиниб, до настоящего времени отсутствует. Не рекомендуется вводить живые вакцины одновременно с тофацитинибом. Рекомендуется, чтобы до начала применения тофацитиниба все пациенты выполнили необходимую иммунизацию в соответствии с современными рекомендациями по вакцинации. Промежуток между вакцинацией живыми вакцинами и началом терапии тофацитинибом должен соответствовать имеющимся руководствам по вакцинации в отношении пациентов, получающих терапию иммуномодулирующими средствами. Согласно этим руководствам, если вводится живая вакцина от опоясывающего герпеса (herpes zoster), ее следует вводить только пациентам с документированным в анамнезе случаем заболевания ветряной оспой или пациентам, серопозитивным в отношении вируса ветряной оспы. Вакцинацию следует проводить по меньшей мере за 2 недели, но предпочтительно за 4 недели до начала терапии иммуномодулирующими средствами, такими как тофацитиниб.
Пациенты с нарушением функции почек
В клинических исследованиях тофацитиниб не изучали у пациентов с исходным клиренсом креатинина менее 40 мл/мин (расчет производился по формуле Кокрофта-Голта) (см. раздел 4.3).
Пациенты с нарушением функции почек или печени или с отклонениями лабораторных показателей
Оценивайте состояние пациентов на исходном уровне и в дальнейшем в соответствии с локальной практикой наблюдения за пациентами. Рекомендации относительно коррекции дозы у пациентов с гематологическими, почечными и печеночными лабораторными отклонениями описаны в разделе 4.2. Проводите терапию и наблюдение за пациентами в соответствии с клиническими рекомендациями.
Пациенты пожилого возраста
Пациенты пожилого возраста, в целом, подвержены повышенному риску возникновения нежелательных явлений, которые имеют более тяжелую степень, поэтому при лечении пациентов пожилого возраста следует соблюдать осторожность (см. раздел 4.8).
Применение у пациентов, которым требуется инвазивная или неинвазивная вентиляция или экстракорпоральная мембранная оксигенация (ЭКМО)
Тофацитиниб изучался только у госпитализированных взрослых пациентов, которым не требовалась неинвазивная вентиляция, инвазивная механическая вентиляция или ЭКМО. Тофацитиниб не должен применяться у пациентов, которым в начале терапии требуется неинвазивная вентиляция, инвазивная механическая вентиляция или ЭКМО. Вспомогательные вещества
Препарат Тофацитиниб Фармасинтез содержит мальтитол, поэтому пациентам с редко встречающейся наследственной непереносимостью фруктозы не следует принимать этот препарат.
Раствор для приема внутрь
Применение в комбинации с другими препаратами
Применение тофацитиниба не изучалось, и его следует избегать в комбинации с биологическими препаратами, такими как антагонисты ФНО, антагонисты интерлейкина (IL)-1R, антагонисты IL-6R, моноклональные антитела к CD20, антагонисты IL-17, антагонисты IL-12/IL-23, антиинтегрины, селективные модуляторы ко-стимуляции и высокоактивные иммунодепрессанты (такие как азатиоприн, 6-меркаптопурин, циклоспорин и такролимус), из-за возможности усиления иммуносупрессии с последующим увеличением риска развития инфекции.
В клинических исследованиях на фоне применения тофацитиниба в комбинации с МТ у пациентов с ревматоидным артритом (РА) наблюдалась более высокая частота возникновения нежелательных реакций, чем при применении тофацитиниба в виде монотерапии.
Применение тофацитиниба в комбинации с ингибиторами фосфодиэстеразы 4 типа не изучалось в клинических исследованиях тофацитиниба.
Венозная тромбоэмболия (ВТЭ)
У пациентов, принимавших тофацитиниб, отмечались серьезные явления ВТЭ, включая тромбоэмболию легочной артерии (ТЭЛА), в некоторых случаях с летальным исходом, а также тромбоз глубоких вен (ТГВ). В рандомизированном пострегистрационном исследовании безопасности у пациентов с РА в возрасте 50 лет или старше по меньшей мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний наблюдалось дозозависимое повышение риска ВТЭ при применении тофацитиниба в сравнении с применением ингибиторов ФНО (см. разделы 4.8 и 5.1).
По результатам апостериорного поискового анализа в рамках данного исследования у пациентов с известными факторами риска ВТЭ случаи последующей ВТЭ наблюдались чаще у пациентов, получавших лечение тофацитинибом, у которых через 12 месяцев лечения уровень D-димера был ≥ 2 × ВГН, чем у пациентов, у которых уровень D-димера был < 2 × ВГН; это не было очевидно у пациентов, получавших лечение ингибиторами ФНО. Интерпретация ограничена малым числом явлений ВТЭ и ограниченной доступностью анализа на D-димер (анализ выполнялся только на исходном уровне, на 12 месяц и в конце исследования). У пациентов, не имеющих ВТЭ во время исследования, средние уровни D-димера были значительно снижены к 12 месяцу по сравнению с исходным уровнем во всех группах лечения. Однако уровни D-димера ≥ 2 × ВГН на 12 месяц наблюдались приблизительно у 30 % пациентов без последующих явлений ВТЭ, что указывает на ограниченную специфичность анализа на D-димер в этом исследовании.
Тофацитиниб следует с осторожностью применять у пациентов с известными факторами риска ВТЭ, независимо от показания к применению и дозы.
Факторы риска ВТЭ включают: наличие ВТЭ в анамнезе, обширное хирургическое вмешательство у пациентов, иммобилизацию, инфаркт миокарда (в течение предыдущих 3 месяцев), сердечную недостаточность, применение комбинированных гормональных контрацептивов или гормонозаместительной терапии, наследственное нарушение свертываемости крови и злокачественные новообразования. Следует также учитывать дополнительные факторы риска ВТЭ, такие как возраст, ожирение (ИМТ ≥ 30), сахарный диабет, артериальная гипертензия, курение. Во время лечения тофацитинибом следует периодически проводить повторную оценку пациентов для анализа изменения риска ВТЭ.
Для пациентов с РА с известными факторами риска ВТЭ следует рассмотреть возможность определения уровней D-димера после приблизительно 12 месяцев лечения. Если результат анализа на D-димер составляет ≥ 2 × ВГН, следует убедиться, что клиническая польза превышает риски до принятия решения о продолжении лечения тофацитинибом.
Необходимо безотлагательно провести оценку пациентов с признаками и симптомами ВТЭ и прекратить применение тофацитиниба у пациентов с подозрением на ВТЭ независимо от дозы или показания к применению.
Тромбоз вен сетчатки глаза
О случаях тромбоза вен сетчатки глаза (ТВСГ) сообщали у пациентов, получавших тофацитиниб (см. раздел 4.8). Пациентам следует рекомендовать оперативно обратиться за медицинской помощью в случае появления симптомов, указывающих на ТВСГ.
Серьезные инфекции
У пациентов, получаюших тофацитиниб, отмечены серьезные, а иногда и смертельные инфекции, вызванные бактериальными, микобактериальными, инвазивными грибковыми, вирусными или иными оппортунистическими возбудителями. Риск возникновения оппортунистических инфекций выше у пациентов, проживающих в регионах Азии (см. раздел 4.8). Пациенты с ревматоидным артритом, принимающие глюкокортикостероиды, могут иметь предрасположенность к развитию инфекций.
Тофацитиниб не следует применять у пациентов с активными инфекциями, включая локальные инфекции.
Перед применением тофацитиниба следует оценить соотношение риск/польза от терапии у пациентов:
- с рецидивирующими инфекциями;
- с наличием тяжелой или оппортунистической инфекции в анамнезе;
- которые жили или недавно посетили эндемичные районы по микозам;
- с сопутствующими патологическими состояниями, которые могут предрасполагать к развитию инфекции.
Пациенты подлежат внимательному наблюдению на предмет развития признаков и симптомов инфекции во время и после терапии тофацитинибом. Лечение следует прервать, если у пациента развивается серьезная инфекция, оппортунистическая инфекция или сепсис. Пациенту, у которого во время лечения тофацитинибом развилась новая инфекция, следует провести быстрое и полное, соответствующее для пациента с ослабленным иммунитетом, диагностическое обследование, следует начать соответствующую противомикробную терапию и обеспечить тщательное наблюдение за пациентом.
Поскольку пациенты с сахарным диабетом обычно характеризуются более высокой частотой развития инфекций, в подобных случаях также следует соблюдать осторожность. (см. раздел 4.8).
Риск инфекции может повышаться при увеличении степени тяжести лимфопении, в этом случае при оценке индивидуального риска развития инфекции следует принимать во внимание число лимфоцитов. Условия отмены препарата и критерии контроля лимфопении описаны в разделе 4.2.
Туберкулез
Перед применением тофацитиниба следует оценить соотношение риск/польза от терапии у пациентов:
- с туберкулезом в анамнезе;
- которые жили или недавно посетили эндемичные районы по туберкулезу.
Перед применением и во время терапии тофацитинибом следует оценить состояние пациента и провести обследование на предмет признаков латентной или активной туберкулезной инфекции в соответствии с локальными рекомендациями.
Пациенты с латентным туберкулезом перед началом терапии тофацитинибом подлежат стандартной антимикобактериальной терапии.
Перед началом терапии тофацитинибом у пациентов с отрицательным результатом исследования на туберкулез, но с латентным или активным туберкулезом в анамнезе, при отсутствии подтверждения адекватного курса противотуберкулезной терапии, а также у пациентов с отрицательным результатом теста, но наличием факторов риска туберкулезной инфекции, следует провести противотуберкулезную терапию. При принятии решения относительно необходимости проведения противотуберкулезной терапии у каждого конкретного пациента рекомендуется проконсультироваться с фтизиатром. Пациенты подлежат тщательному наблюдению на предмет развития признаков и симптомов туберкулеза, включая пациентов с отрицательным результатом теста на латентный туберкулез до начала терапии.
Реактивация вирусных инфекций
Случаи реактивации вирусных инфекций, включая случаи реактивации вируса герпеса (например, опоясывающего герпеса), наблюдались у пациентов, получавших тофацитиниб (см. раздел 4.8).
При лечении тофацитинибом частота появления опоясывающего герпеса может увеличиться:
- у пациентов японской или корейской национальностей;
- у пациентов с АЧЛ менее 1000 клеток/мм3 (см. раздел 4.2);
- у пациентов с длительным анамнезом РА, которые ранее получали два или более БПВП.
Влияние тофацитиниба на реактивацию хронического вирусного гепатита неизвестно. Пациентов с положительным результатом тестирования на гепатиты B или C при скрининге исключали из клинических исследований. Перед началом терапии тофацитинибом следует провести скрининг на предмет наличия вирусного гепатита в соответствии с клиническими рекомендациями.
Основные нежелательные сердечно-сосудистые события (MACE) (включая инфаркт миокарда)
У пациентов, получавших тофацитиниб, наблюдались основные нежелательные сердечно- сосудистые события (MACE).
В рандомизированном пострегистрационном исследовании безопасности у пациентов с РА в возрасте 50 лет или старше, по меньшей мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний, наблюдалось увеличение частоты возникновения инфаркта миокарда при применении тофацитиниба по сравнению с ингибиторами ФНО (см. разделы 4.8 и 5.1). У пациентов, которые курят или курили в прошлом, и у пациентов с другими факторами риска сердечно-сосудистых заболеваний тофацитиниб следует применять только при отсутствии других подходящих альтернативных методов лечения.
Злокачественные новообразования и лимфопролиферативные заболевания
Тофацитиниб может неблагоприятно влиять на механизмы защиты организма от злокачественных новообразований.
В рандомизированном пострегистрационном исследовании безопасности у пациентов с РА в возрасте 50 лет или старше по меньшей мере с одним дополнительным фактором риска сердечно-сосудистых заболеваний наблюдалось повышение частоты возникновения злокачественных новообразований, кроме рака кожи, не относящегося к меланоме (РКНМ), особенно рака легкого и лимфомы, при применении тофацитиниба по сравнению с ингибиторами ФНО (см. разделы 4.8 и 5.1).
В других клинических исследованиях и в пострегистрационном периоде применения препарата также наблюдались случаи развития рака легкого и лимфомы у пациентов, получавших тофацитиниб.
В клинических исследованиях и в пострегистрационном периоде были зарегистрированы случаи развития других злокачественных новообразований, включая, но не ограничиваясь, рак молочной железы, меланому, рак предстательной железы и рак поджелудочной железы.
У пациентов, которые курят или курили в прошлом, и у пациентов с другими факторами риска злокачественных новообразований (например, злокачественное новообразование на момент лечения или злокачественное новообразование в анамнезе, кроме успешно излеченного РКНМ) тофацитиниб следует применять только при отсутствии подходящих альтернативных методов лечения.
Рак кожи, не относящийся к меланоме (РКНМ)
У пациентов, получавших тофацитиниб, сообщалось о случаях РКНМ. Риск развития РКНМ может быть выше у пациентов, получающих тофацитиниб в дозе 10 мг два раза в день, по сравнению с пациентами, получающими тофацитиниб в дозе 5 мг два раза в день. Пациентам с повышенным риском возникновения рака кожи рекомендуется периодически проводить обследование кожи (см. таблицу 7 в разделе 4.8).
Интерстициальная болезнь легких
Также рекомендуется соблюдать осторожность у пациентов с наличием в анамнезе хронического заболевания легких, поскольку они могут быть более склонны к инфекциям. У пациентов, получавших тофацитиниб в клинических исследованиях при РА и в условиях пострегистрационного применения, были зарегистрированы явления интерстициальной болезни легких (некоторые из них — с летальным исходом), хотя роль ингибирования янус- киназы (JAK) в развитии этих явлений неизвестна. Известно, что пациенты азиатского происхождения подвержены повышенному риску развития интерстициальной болезни легких, поэтому при лечении этих пациентов следует проявлять осторожность.
Случаи перфорации органов ЖКТ
В клинических исследованиях описаны случаи перфорации органов желудочно-кишечного тракта, хотя роль ингибирования JAK при этих явлениях неизвестна. Тофацитиниб следует с осторожностью применять у пациентов с повышенным риском перфорации органов желудочно-кишечного тракта (например, у пациентов с дивертикулитом в анамнезе и пациентов, получающих сопутствующую терапию кортикостероидами и /или нестероидными противовоспалительными средствами (НПВС)). Пациенты с новыми симптомами со стороны брюшной полости, подлежат немедленному обследованию для раннего выявления перфорации органов желудочно-кишечного тракта.
Переломы
У пациентов, получавших лечение тофацитинибом, были зарегистрированы переломы.
Тофацитиниб следует применять с осторожностью у пациентов с известными факторами риска переломов, например у пожилых пациентов, женщин и пациентов, получающих кортикостероиды, независимо от показания и режима дозирования.
Печеночные ферменты
При лечении тофацитинибом у некоторых пациентов наблюдалось увеличение частоты повышения уровней печеночных ферментов (см. раздел 4.8 «Анализы для определения уровней печеночных ферментов»). Следует с вниманием подходить к вопросу о начале лечения тофацитинибом у пациентов с повышенными уровнями аланинаминотрансферазы (АЛТ) или аспартатаминотрансферазы (АСТ), особенно при начале применения препарата в комбинации с потенциально гепатотоксичными лекарственными препаратами, такими как МТ. После начала лечения для выявления потенциальных случаев лекарственного поражения печени рекомендуется осуществлять на постоянной основе контроль биохимических показателей функции печени и быстро устанавливать возможные причины повышения уровней печеночных ферментов. Если подозревается лекарственное поражение печени, лечение тофацитинибом следует приостановить до исключения этого диагноза.
Гиперчувствительность
В пострегистрационном периоде наблюдались случаи реакций гиперчувствительности на фоне применения тофацитиниба. Аллергические реакции включали ангионевротический отек и крапивницу; некоторые случаи оценивались как серьезные. В случае возникновения серьезной анафилактической реакции или реакции гиперчувствительности необходимо немедленно прекратить применение тофацитиниба.
Лабораторные показатели
Лимфоциты
При лечении тофацитинибом наблюдалась более высокая частота возникновения лимфопении по сравнению с плацебо. Случаи снижения числа лимфоцитов до уровня менее 750 клеток/мм3 были связаны с увеличением частоты возникновения серьезных инфекций. Не рекомендуется начинать или продолжать терапию тофацитинибом у пациентов с подтвержденным числом лимфоцитов менее 750 клеток/мм3. Число лимфоцитов следует контролировать на исходном уровне, а затем каждые 3 месяца. Рекомендации по изменению дозы в зависимости от числа лимфоцитов представлены в разделе 4.2.
Нейтрофилы
Лечении тофацитинибом сопровождалось увеличением частоты развития нейтропении (менее 2000 клеток/мм3) по сравнению с плацебо. Начинать лечение тофацитинибом при АЧН менее 1000 клеток/мм3 у взрослых пациентов и при АЧН менее 1200 клеток/мм3 у детей не рекомендуется. АЧН следует контролировать на исходном уровне, после 4– 8 недель терапии, а затем каждые 3 месяца. Рекомендации по изменению дозы в зависимости от АЧН приведены в разделе 4.2.
Гемоглобин
При лечении тофацитинибом наблюдалось снижение уровня гемоглобина. Не рекомендуется начинать терапию тофацитинибом при уровне гемоглобина менее 9 г/дл у взрослых пациентов и менее 10 г/дл у детей. Уровень гемоглобина следует контролировать на начальном этапе терапии, после 4–8 недель лечения, а затем каждые 3 месяца. Рекомендации по изменению дозы в зависимости от уровня гемоглобина приведены в разделе 4.2.
Мониторинг уровня липидов
Лечение тофацитинибом сопровождается повышением уровня липидов крови – общего холестерина, холестерина липопротеинов низкой плотности (ЛПНП), а также холестерина липопротеинов высокой плотности (ЛПВП). Максимальный эффект обычно отмечался в течение 6 недель. Оценку липидных параметров следует выполнять по прошествии 8 недель после начала терапии тофацитинибом. Лечение пациентов необходимо проводить в соответствии с клиническими рекомендациями по лечению гиперлипидемии. Применение статинов у пациентов с повышенной концентрацией общего холестерина и холестерина ЛПНП на фоне терапии тофацитинибом позволяет достичь исходных показателей.
Гипогликемия у пациентов, получавших препараты для лечения диабета
Сообщалось о случаях гипогликемии после начала терапии тофацитинибом у пациентов, получавших препараты для лечения диабета. В случае гипогликемии может потребоваться корректировка дозы противодиабетического препарата.
Вакцинации
Рекомендуется, чтобы до начала применения тофацитиниба все пациенты, особенно с полиартикулярным ювенильным идиопатическим артритом (пЮИА) и ювенильным псориатическим артритом (ЮПсА), выполнили необходимую иммунизацию в соответствии с современными рекомендациями по вакцинации. Не рекомендуется вводить живые вакцины одновременно с тофацитинибом. При принятии решения о применении живых вакцин до начала лечения тофацитинибом следует учитывать наличие иммуносупрессии у соответствующего пациента.
Проведение профилактической вакцинации против опоясывающего герпеса следует рассматривать в соответствии с рекомендациями по вакцинации. Следует с особым вниманием относиться к пациентам с длительно текущим РА, которые ранее получали лечение двумя или более биологическими БПВП. Если вводится живая вакцина от опоясывающего герпеса (herpes zoster), ее следует вводить только пациентам c документированным в анамнезе случаем заболевания ветряной оспой или пациентам, серопозитивным в отношении вируса ветряной оспы (ВВО). Если сведения о наличии ветряной оспы в анамнезе считаются сомнительными или ненадежными, рекомендуется провести анализ на наличие антител к ВВО.
Вакцинацию живыми вакцинами следует проводить по меньшей мере за 2 недели, а предпочтительно за 4 недели до начала терапии тофацитинибом или в соответствии с современными рекомендациями по вакцинации, касающимися применения иммуномодулирующих лекарственных средств. Данные о вторичной передаче инфекции при введении живых вакцин пациентам, получающим лечение тофацитинибом, отсутствуют.
Содержание вспомогательных веществ
Пропиленгликоль
В 1 мг данного лекарственного препарата содержится 2,39 мг пропиленгликоля.
Ниже приведены примеры расчета уровня воздействия пропиленгликоля в зависимости от суточной дозы препарата (см. раздел 4.2).
- При применении препарата Яквинус раствор для приема внутрь 1 мг/мл в дозе 3,2 мг два раза в день у детей с массой тела от 10 до < 20 кг уровень воздействия пропиленгликоля составит 1,53 мг/кг/сут.
- При применении препарата Яквинус раствор для приема внутрь 1 мг/мл в дозе 4 мг два раза в день у детей с массой тела от 20 до < 40 кг уровень воздействия пропиленгликоля составит 0,96 мг/кг/сут.
- При применении препарата Яквинус раствор для приема внутрь 1 мг/мл в дозе 5 мг два раза в день у детей с массой тела ≥ 40 кг уровень воздействия пропиленгликоля составит 0,60 мг/кг/сут.
Натрия бензоат
В 1 мл данного лекарственного препарата содержится 0,9 мг бензоата натрия.
Натрий
В 1 мл данного лекарственного препарата содержится менее 1 ммоль (23 мг) натрия, т. е. препарат практически не содержит натрия.
Влияние не способность управлять транспортными средствами и механизмами
Таблетки
Исследования влияния тофацитиниба на способность к управлению автомобилем и работе с механизмами не проводились.
Раствор для приема внутрь
Яквинус не оказывает влияния на способность к управлению транспортными средствами и работать с механизмами или оказывает несущественное влияние.
Информация для данной статьи взята из инструкций к препаратам тофацитиниба:
- Тофацитиниб Фармасинтез, таблетки покрытые пленочной оболочкой
- Яквинус, раствор для приема внутрь
